Cell Therapeutics vor Tounaround?
21.10.13 19:58
#926
Heron
Studien-Ergebnisse
Cell Therapeutics meldet Ergebnisse aus präklinischen Studie Pixantrone (Pixuvri ®) auf der AACR-NCI-EORTC Konferenz Präsentiert
http://finance.yahoo.com/news/...s-results-preclinical-053000456.html
- Ergebnisse deuten neue Klasse von Anti-Krebs-Agenten mit neuen Mechanismus der Abtötung von Tumorzellen -
SEATTLE, 21. Oktober 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute die Präsentation der Ergebnisse aus einer präklinischen Studie von Pixuvri ® (pixantrone), die den Mechanismus der Induktion Tumor vorschlagen Zelltod ist neu und der sich von dem Anthracycline wie Doxorubicin. Pixuvri ist ein First-in-Class-Aza-anthracenedione mit einzigartigen strukturellen und physikalisch-chemischen Eigenschaften, die derzeit in der Europäischen Union ist für den Einsatz als Monotherapie zur Behandlung von erwachsenen Patienten mit mehrfach rezidivierten oder refraktären aggressiven B-Zell-Non-Hodgkin-Lymphom zugelassen. Die Ergebnisse der Studie wurden von Neil Beeharry, Ph.D., am Fox Chase Cancer Center während einer Poster-Session auf der AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics gehalten 19. bis 23. Oktober 2013 in Boston, MA vorgestellt .
"Die Ergebnisse der Studie legen nahe, dass Pixuvri einzigartig in seiner Mechanismus zur Induktion Tumor Zelltod und unterstützt damit die These, dass es das erste zugelassene Medikament in einer neuen Klasse von Anti-Krebs-Mittel ist. Pixuvri der Wirkmechanismus von der zytotoxische Wirkung induziert wird differenziert von Anthrazyklinen und könnte die Grundlage für die Wirksamkeit und Sicherheit des Medikaments sein ", erklärte Dr. Beeharry.
Die Studie wurde der Mechanismus der Abtötung von Tumorzellen durch Pixuvri in einer Vielzahl von Zelllinien induziert. Insbesondere ist die Untersuchung der Auswirkungen Pixuvri hatte auf die Zellproliferation und Zeit beurteilt, um den Zelltod bewirkt der Zellzyklus, die DNA-Reparatur-und langfristig auf die Zellteilung. Im Gegensatz zu Anthrazyklinen - die töten normalen und Krebszellen mit kurzfristigen Exposition - Pixuvri hatte minimale kurzfristige Auswirkungen auf das Überleben der Zelle, aber wahrscheinlich durch Bildung stabiler DNA-Addukte, Verzögert, aber effiziente Tumorzelltod. Dieser Effekt war nicht abhängig von der Anwesenheit des p53-Gen, ein Gen mit der Anerkennung Chromosomenschädigung und Apoptose. Verlust von p53 wurde nur mit einer weiteren Verzögerung in Zelltod mit längeren Exposition gegenüber Pixuvri verbunden. Die Autoren schlossen daraus, dass Pixuvri zu beeinträchtigen Chromosomentrennung sein scheint während der Mitose, wodurch Verlust an genetischem Material in Tochterzellen, eine Anomalie, die letztlich tödlich ist, und dass Pixuvri wahrscheinlich wirksam in Zellen gegenüber anderen Zytostatika wie Doxorubicin. Die Autoren verfolgen führt zu weiteren Verständnis der genaue Wirkmechanismus.
Der vollständige Poster-Präsentation ist online verfügbar unter www.celltherapeutics.com / publications .
Über Pixuvri (pixantrone)
Pixuvri ist ein neuartiges Aza-anthracenedione mit einzigartigen strukturellen und physikalisch-chemischen Eigenschaften. Im Gegensatz zu verwandten Verbindungen bildet Pixuvri stabile DNA-Addukte und in präklinischen Modellen eine deutlich höhere Anti-Lymphom-Aktivität im Vergleich zu verwandten Verbindungen. Pixuvri wurde baulich so konzipiert, dass sie nicht binden können Eisen-und verewigen Sauerstoffradikale Produktion oder bilden eine langlebige Hydroxy-Metaboliten - die beide die mutmaßlichen Mechanismen für die Anthrazyklin-induzierte akute und chronische Kardiotoxizität sind. Diese neuartigen pharmakologischen Eigenschaften erlauben Pixuvri, um Patienten mit einer nahezu maximalen lebenslanger Exposition gegenüber Anthrazykline ohne dass die Kardiotoxizität inakzeptabel verabreicht werden.
Im Mai 2012 hat die Europäische Kommission (EC) eine bedingte Zulassung für Pixuvri als Monotherapie zur Behandlung von erwachsenen Patienten mit rezidivierten oder refraktären aggressiven NHL mehrfach. Der Vorteil der Pixuvri Behandlung wurde bei Patienten festgestellt, wenn sie als fünfte Zeile oder größer Chemotherapie bei Patienten, die refraktär gegen die vorausgegangene Therapie eingesetzt. Die Zusammenfassung der Merkmale des Arzneimittels (Fachinformation) hat die vollständige Fachinformation, einschließlich der Sicherheit und Wirksamkeit von Pixuvri in der zugelassenen Indikation. Die Fachinformation finden Sie unter www.pixuvri.eu .
CTI ist derzeit anfallenden Patienten in einer Phase-3-Studie zum Vergleich von Pixuvri und Rituximab mit Gemcitabin und Rituximab in der Einstellung von aggressiven B-Zell-NHL. Pixuvri keine Marktzulassung in den Vereinigten Staaten.
Über Cell Therapeutics, Inc.
CTI (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Forward-Looking Statements
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, von denen wesentlich und / oder nachteilig auf die tatsächlichen zukünftigen Ergebnisse und den Börsenkurs der CTI Wertpapiere. Solche Aussagen umfassen, sind aber nicht beschränkt auf, Aussagen in Bezug auf die Erwartungen in Bezug auf die Entwicklung des Unternehmens und seiner Produkte und Produkt-Kandidat Portfolio, das Pixuvri ist einzigartig in seiner Mechanismus zur Induktion Tumorzelltod beschränkt und unterstützt damit die These, dass es ein Teil ist einer neuen Klasse von Anti-Krebs-Mittel und leicht aus dem Wirkmechanismus mit Anthrazyklinen verbunden differenziert, und dass Pixuvri verzögert, aber effiziente Tumorzelltod wahrscheinlich dazu führen, durch Bildung stabiler DNA-Addukte. Risiken, die mit der unsicheren Natur der zukunftsgerichteten Aussagen beitragen, gehören unter anderem Risiken, dass Pixuvri nicht zu beweisen, sicher und wirksam für die Behandlung von rezidivierender oder refraktärer NHL und / oder anderen Tumoren, dass die Ergebnisse in künftigen Studien oder die tatsächlichen Ergebnisse von Pixuvri kann aus den Ergebnissen der früheren Studien unterscheiden; die CTI möglicherweise nicht in der Lage komplette ein Post-Marketing-Studie bestätigt den klinischen Nutzen in der Studie beobachtete PIX301 gerichtet sein; dass die bedingte Zulassung von Pixuvri kann nicht verlängert werden; dass CTI may keine günstigen Kostenerstattung oder Preisbildung Bestimmungen für Pixuvri in bestimmten Märkten in der EU wie geplant, und Risiken im Zusammenhang mit der biopharmazeutischen Industrie im Allgemeinen und mit CTI und seine Produkt-und Produkt-Kandidat Portfolio insbesondere auch, unter anderem, Risiken im Zusammenhang mit der folgenden assoziiert: dass CTI können nicht vorhersagen oder garantieren das Tempo oder Geographie der Einschreibung ihrer klinischen Studien, dass die zweite Phase 3 klinischen Studie pacritinib wird nicht auftreten, wie geplant, das CTI nicht gestattet günstigen Bestimmungen durch andere Regulierungs-, Patent-und Verwaltungsbehörden, dass CTI kann es zu Verzögerungen bei der Aufnahme der präklinischen und klinischen Studien, Risiken im Zusammenhang mit den Kosten für die Entwicklung, Herstellung und Verkauf Pixuvri pacritinib und CTI anderen Produkt-Kandidaten, sowie andere Risiken, einschließlich, ohne Einschränkung, Wettbewerbsfaktoren, technologische Entwicklungen, dass CTI Betriebsausgaben weiterhin seine Erträge, die CTI nicht in der Lage, seine aktuellen Kostenkontrolle erhalten oder weiter zu reduzieren ihre Betriebskosten, dass CTI nicht erreichen angekündigten Ziele wie oder bei der Projektion, dass CTI durchschnittlichen operativen brennen überschreiten Rate erhöhen, dass CTI weiterhin brauchen, um Kapital aufzubringen, um die Betriebskosten zu finanzieren, kann aber nicht in der Lage, ausreichende Mengen zu erhöhen, um deren weiterer Betrieb sowie andere Risiken aufgeführt oder von Zeit beschrieben, um Zeit zu finanzieren in den neuesten Einreichungen von CTI bei der Securities and Exchange Commission auf den Formularen 10-K, 10-Q und 8-K. Sofern nicht gesetzlich vorgeschrieben, übernimmt CTI nicht die Absicht, eine der Aussagen in dieser Pressemitteilung auf weitere Entwicklungen zu aktualisieren.
Pixuvri ist ein eingetragenes Warenzeichen von Cell Therapeutics, Inc.
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206-282-7100
ebell@ctiseattle.com
In Europa:
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
+39 02 89659706
lvilla@cti-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
http://finance.yahoo.com/news/...s-results-preclinical-053000456.html
- Ergebnisse deuten neue Klasse von Anti-Krebs-Agenten mit neuen Mechanismus der Abtötung von Tumorzellen -
SEATTLE, 21. Oktober 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute die Präsentation der Ergebnisse aus einer präklinischen Studie von Pixuvri ® (pixantrone), die den Mechanismus der Induktion Tumor vorschlagen Zelltod ist neu und der sich von dem Anthracycline wie Doxorubicin. Pixuvri ist ein First-in-Class-Aza-anthracenedione mit einzigartigen strukturellen und physikalisch-chemischen Eigenschaften, die derzeit in der Europäischen Union ist für den Einsatz als Monotherapie zur Behandlung von erwachsenen Patienten mit mehrfach rezidivierten oder refraktären aggressiven B-Zell-Non-Hodgkin-Lymphom zugelassen. Die Ergebnisse der Studie wurden von Neil Beeharry, Ph.D., am Fox Chase Cancer Center während einer Poster-Session auf der AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics gehalten 19. bis 23. Oktober 2013 in Boston, MA vorgestellt .
"Die Ergebnisse der Studie legen nahe, dass Pixuvri einzigartig in seiner Mechanismus zur Induktion Tumor Zelltod und unterstützt damit die These, dass es das erste zugelassene Medikament in einer neuen Klasse von Anti-Krebs-Mittel ist. Pixuvri der Wirkmechanismus von der zytotoxische Wirkung induziert wird differenziert von Anthrazyklinen und könnte die Grundlage für die Wirksamkeit und Sicherheit des Medikaments sein ", erklärte Dr. Beeharry.
Die Studie wurde der Mechanismus der Abtötung von Tumorzellen durch Pixuvri in einer Vielzahl von Zelllinien induziert. Insbesondere ist die Untersuchung der Auswirkungen Pixuvri hatte auf die Zellproliferation und Zeit beurteilt, um den Zelltod bewirkt der Zellzyklus, die DNA-Reparatur-und langfristig auf die Zellteilung. Im Gegensatz zu Anthrazyklinen - die töten normalen und Krebszellen mit kurzfristigen Exposition - Pixuvri hatte minimale kurzfristige Auswirkungen auf das Überleben der Zelle, aber wahrscheinlich durch Bildung stabiler DNA-Addukte, Verzögert, aber effiziente Tumorzelltod. Dieser Effekt war nicht abhängig von der Anwesenheit des p53-Gen, ein Gen mit der Anerkennung Chromosomenschädigung und Apoptose. Verlust von p53 wurde nur mit einer weiteren Verzögerung in Zelltod mit längeren Exposition gegenüber Pixuvri verbunden. Die Autoren schlossen daraus, dass Pixuvri zu beeinträchtigen Chromosomentrennung sein scheint während der Mitose, wodurch Verlust an genetischem Material in Tochterzellen, eine Anomalie, die letztlich tödlich ist, und dass Pixuvri wahrscheinlich wirksam in Zellen gegenüber anderen Zytostatika wie Doxorubicin. Die Autoren verfolgen führt zu weiteren Verständnis der genaue Wirkmechanismus.
Der vollständige Poster-Präsentation ist online verfügbar unter www.celltherapeutics.com / publications .
Über Pixuvri (pixantrone)
Pixuvri ist ein neuartiges Aza-anthracenedione mit einzigartigen strukturellen und physikalisch-chemischen Eigenschaften. Im Gegensatz zu verwandten Verbindungen bildet Pixuvri stabile DNA-Addukte und in präklinischen Modellen eine deutlich höhere Anti-Lymphom-Aktivität im Vergleich zu verwandten Verbindungen. Pixuvri wurde baulich so konzipiert, dass sie nicht binden können Eisen-und verewigen Sauerstoffradikale Produktion oder bilden eine langlebige Hydroxy-Metaboliten - die beide die mutmaßlichen Mechanismen für die Anthrazyklin-induzierte akute und chronische Kardiotoxizität sind. Diese neuartigen pharmakologischen Eigenschaften erlauben Pixuvri, um Patienten mit einer nahezu maximalen lebenslanger Exposition gegenüber Anthrazykline ohne dass die Kardiotoxizität inakzeptabel verabreicht werden.
Im Mai 2012 hat die Europäische Kommission (EC) eine bedingte Zulassung für Pixuvri als Monotherapie zur Behandlung von erwachsenen Patienten mit rezidivierten oder refraktären aggressiven NHL mehrfach. Der Vorteil der Pixuvri Behandlung wurde bei Patienten festgestellt, wenn sie als fünfte Zeile oder größer Chemotherapie bei Patienten, die refraktär gegen die vorausgegangene Therapie eingesetzt. Die Zusammenfassung der Merkmale des Arzneimittels (Fachinformation) hat die vollständige Fachinformation, einschließlich der Sicherheit und Wirksamkeit von Pixuvri in der zugelassenen Indikation. Die Fachinformation finden Sie unter www.pixuvri.eu .
CTI ist derzeit anfallenden Patienten in einer Phase-3-Studie zum Vergleich von Pixuvri und Rituximab mit Gemcitabin und Rituximab in der Einstellung von aggressiven B-Zell-NHL. Pixuvri keine Marktzulassung in den Vereinigten Staaten.
Über Cell Therapeutics, Inc.
CTI (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Forward-Looking Statements
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, von denen wesentlich und / oder nachteilig auf die tatsächlichen zukünftigen Ergebnisse und den Börsenkurs der CTI Wertpapiere. Solche Aussagen umfassen, sind aber nicht beschränkt auf, Aussagen in Bezug auf die Erwartungen in Bezug auf die Entwicklung des Unternehmens und seiner Produkte und Produkt-Kandidat Portfolio, das Pixuvri ist einzigartig in seiner Mechanismus zur Induktion Tumorzelltod beschränkt und unterstützt damit die These, dass es ein Teil ist einer neuen Klasse von Anti-Krebs-Mittel und leicht aus dem Wirkmechanismus mit Anthrazyklinen verbunden differenziert, und dass Pixuvri verzögert, aber effiziente Tumorzelltod wahrscheinlich dazu führen, durch Bildung stabiler DNA-Addukte. Risiken, die mit der unsicheren Natur der zukunftsgerichteten Aussagen beitragen, gehören unter anderem Risiken, dass Pixuvri nicht zu beweisen, sicher und wirksam für die Behandlung von rezidivierender oder refraktärer NHL und / oder anderen Tumoren, dass die Ergebnisse in künftigen Studien oder die tatsächlichen Ergebnisse von Pixuvri kann aus den Ergebnissen der früheren Studien unterscheiden; die CTI möglicherweise nicht in der Lage komplette ein Post-Marketing-Studie bestätigt den klinischen Nutzen in der Studie beobachtete PIX301 gerichtet sein; dass die bedingte Zulassung von Pixuvri kann nicht verlängert werden; dass CTI may keine günstigen Kostenerstattung oder Preisbildung Bestimmungen für Pixuvri in bestimmten Märkten in der EU wie geplant, und Risiken im Zusammenhang mit der biopharmazeutischen Industrie im Allgemeinen und mit CTI und seine Produkt-und Produkt-Kandidat Portfolio insbesondere auch, unter anderem, Risiken im Zusammenhang mit der folgenden assoziiert: dass CTI können nicht vorhersagen oder garantieren das Tempo oder Geographie der Einschreibung ihrer klinischen Studien, dass die zweite Phase 3 klinischen Studie pacritinib wird nicht auftreten, wie geplant, das CTI nicht gestattet günstigen Bestimmungen durch andere Regulierungs-, Patent-und Verwaltungsbehörden, dass CTI kann es zu Verzögerungen bei der Aufnahme der präklinischen und klinischen Studien, Risiken im Zusammenhang mit den Kosten für die Entwicklung, Herstellung und Verkauf Pixuvri pacritinib und CTI anderen Produkt-Kandidaten, sowie andere Risiken, einschließlich, ohne Einschränkung, Wettbewerbsfaktoren, technologische Entwicklungen, dass CTI Betriebsausgaben weiterhin seine Erträge, die CTI nicht in der Lage, seine aktuellen Kostenkontrolle erhalten oder weiter zu reduzieren ihre Betriebskosten, dass CTI nicht erreichen angekündigten Ziele wie oder bei der Projektion, dass CTI durchschnittlichen operativen brennen überschreiten Rate erhöhen, dass CTI weiterhin brauchen, um Kapital aufzubringen, um die Betriebskosten zu finanzieren, kann aber nicht in der Lage, ausreichende Mengen zu erhöhen, um deren weiterer Betrieb sowie andere Risiken aufgeführt oder von Zeit beschrieben, um Zeit zu finanzieren in den neuesten Einreichungen von CTI bei der Securities and Exchange Commission auf den Formularen 10-K, 10-Q und 8-K. Sofern nicht gesetzlich vorgeschrieben, übernimmt CTI nicht die Absicht, eine der Aussagen in dieser Pressemitteilung auf weitere Entwicklungen zu aktualisieren.
Pixuvri ist ein eingetragenes Warenzeichen von Cell Therapeutics, Inc.
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206-282-7100
ebell@ctiseattle.com
In Europa:
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
+39 02 89659706
lvilla@cti-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
23.10.13 20:00
#927
Heron
Info
Cell Therapeutics to Report Third Quarter Financial Results after Market on October 30, 2013
- Conference call and webcast at 4:30 p.m. Eastern Time -
Wednesday, October 30, 2013
1:30 p.m. PDT/4:30 p.m. EDT/10:30 p.m. CEST
http://finance.yahoo.com/news/...-report-third-quarter-053000200.html
- Conference call and webcast at 4:30 p.m. Eastern Time -
Wednesday, October 30, 2013
1:30 p.m. PDT/4:30 p.m. EDT/10:30 p.m. CEST
http://finance.yahoo.com/news/...-report-third-quarter-053000200.html
30.10.13 22:27
#928
Heron
QIII-Zahlen
Cell Therapeutics für das dritte Quartal 2013 Financial Results
http://finance.yahoo.com/news/...reports-third-quarter-200000798.html
SEATTLE, 30. Oktober 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute die Finanzergebnisse für das dritte Quartal und die neun Monate zum 30. September 2013 bestellen.
"Wir haben vor kurzem erreicht einen wichtigen klinischen Meilenstein in unserer Entwicklung pacritinib Programm, nachdem eine Einigung mit der FDA auf einem Special Protocol Assessment (SPA) für die geplante Phase-3-PERSIST-2-Studie von pacritinib für Patienten mit Myelofibrose, die niedrige Thrombozyten haben ", sagte James Bianco, MD, Präsident und CEO von CTI. "Mit der SPA im Ort, erwarten wir, diese Studie im vierten Quartal 2013 zu initiieren und zu antizipieren Abschluss Einschreibung in etwa 12 Monaten. Wir weiterhin Fortschritte bei der Erstattung Verfahren zur PIXVURI in der Europäischen Union zu machen und sind auf Fortbildung von Ärzten, konzentrierte sich auf die nicht gedeckten medizinischen Bedarf und Gebäude Markenbekanntheit für Pixuvri als dritten und vierten-Line-Behandlung Option unter den Ärzten in Ländern, in denen Pixuvri derzeit verfügbar ist. "
Drittes Quartal 2013 sowie Schlagzeilen
Pixuvri ® (pixantrone) Commercial: Market Access in Frankreich und Italien gewährt
Berichtet, dass das Unternehmen den Marktzugang wurde von der Kommission Transparenz des Französisch National Health Authority in Frankreich und von der italienischen Arzneimittelbehörde (AIFA) in Italien für Pixuvri gewährt als Monotherapie zur Behandlung von erwachsenen Patienten mit mehrfach rezidivierten oder refraktären aggressiven B- Zell-NHL (Patienten mit aggressiven B-Zell-NHL, die 2 oder 3 vorherige Behandlungen fehlgeschlagen).
Forschung und Entwicklung: Erreichte SPA-Abkommen mit FDA für PERSIST-2 Clinical Trial
Einigung mit der US Food and Drug Administration (FDA) auf einem SPA für die geplante Phase-3-Studie, als PERSIST-2 bekannt, Auswertung pacritinib Vergleich zum besten verfügbaren Therapie, einschließlich genehmigt JAK2-Inhibitoren wie ruxolitinib, bei Patienten mit Myelofibrose deren Blutplättchen sind
Firmenintern: Expanded CTI des Wissenschaftlichen Beirats und angehoben Etwa 15 Millionen Dollar Finanzierung.
Hinzugefügt drei Staats-und Regierungschefs in der Forschung und Entwicklung von neuen Therapien für Blut-Krebsarten vor kurzem gebildet Scientific CTI Advisory Board (SAB): Alan List, MD, Präsident und CEO von Moffitt Cancer Center; Ross Levine, MD, Associate Oberarzt am Memorial Sloan-Kettering Cancer Center, und Brian Druker, MD, Direktor des Ritters Cancer Institute an der Oregon Health & Science University. CTI SAB wird von Daniel Von Hoff, MD, BMZ Vorsitz
Abgeschlossen eingetragenen direkten Angebot ohne Underwriter oder Placement Agent für Nettoerlös von rund $ 14.800.000.
Third Quarter 2013 Financial Results
Der Gesamtumsatz für das dritte Quartal und die ersten neun Monate zum 30. September 2013 waren 0.400.000 $ und $ 1,8 Mio. bzw.. Die Einnahmen waren ausschließlich auf Netto-Produktverkäufe von Pixuvri. CTI Pixuvri verkauft direkt an Anbietern von Gesundheitsleistungen und durch eine begrenzte Zahl von Großhändlern in der EU im Allgemeinen zeichnet CTI Produktverkäufe nach Erhalt der Ware durch den Arzt oder Vertreiber, abzüglich Händler Rabatte, geschätzt staatlich verordneten Preisnachlässe und Rabatte, und geschätzte Retouren. Alle künftigen Einnahmen sind abhängig von der Marktakzeptanz Pixuvri, die Entscheidungen über Erstattung von staatlichen Behörden in jedem Land, in dem Pixuvri steht zum Verkauf und andere Faktoren gemacht.
Der operative Verlust für das dritte Quartal 2013 betrug $ 15,6 Mio. im Vergleich zu $ 15.100.000 für den gleichen Zeitraum im Jahr 2012. Für die ersten neun Monate des Jahres 2013 war der operative Verlust $ 51.900.000 gegenüber $ 82.600.000 für den gleichen Zeitraum im Jahr 2012. Der Betrag für die neun Monate zum 30. September aufgezeichnet, inklusive 2012 ein $ 29.100.000 Aufwendungen für erworbene in Arbeit befindliche Forschung und Entwicklung im Zusammenhang mit dem Erwerb von pacritinib von S * BIO Pte Ltd Non-cash, aktienbasierte Vergütungen beliefen sich im dritten Quartal und die ersten neun Monate 2013 betrug $ 1.900.000 und $ 6,3 Mio., verglichen zu $ 1,0 Mio. und $ 6.100.000 für den gleichen Zeitraum im Jahr 2012.
Der Nettoverlust für das dritte Quartal 2013 war $ 22.400.000 oder ($ 0.20) pro Aktie, verglichen mit $ 20.200.000 oder ($ 0,38) je Aktie für den gleichen Zeitraum im Jahr 2012. Für die ersten neun Monate des Jahres 2013, war Nettoverlust $ 59.800.000 oder ($ 0,55) pro Aktie, verglichen mit $ 96.200.000 oder ($ 2.12) pro Aktie für den gleichen Zeitraum im Jahr 2012.
Zum 30. September 2013, betrug CTI Zahlungsmittel und Zahlungsmitteläquivalente $ 27.200.000.
Finanzprognose für das Jahr 2013
CTI bekräftigt vor finanzielle Führung, dass für das Jahr 2013, Betriebsergebnis abzüglich unbare, aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, wird erwartet, dass rund $ 60 bis $ 65.000.000 zu sein. Year-to-date für die ersten neun Monate zum 30. September 2013, des Betriebsergebnisses, ohne nicht zahlungswirksame aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, war $ 45.500.000. Für weitere Informationen über CTI Verwendung dieser nicht GAAP-konformen Kennzahlen und eine Überleitung Non-GAAP-Betriebsergebnis abzüglich unbare aktienbasierte Vergütungen, um den Verlust aus dem operativen Geschäft für die neun Monate zum 30. September 2013, finden Sie im Abschnitt unter dem Titel "Non-GAAP-konformen Finanzkennzahlen".
Tatsächlichen finanziellen Ergebnisse für das Jahr 2013 wird von vielen Faktoren ab, einschließlich des Grades der Marktakzeptanz und Bestimmung der Erstattungssätze für Pixuvri in der EU, die Rate der Patientenrekrutierung in klinischen Studien, die pacritinib laufenden und geplanten für die Initiierung im Jahr 2013 und andere Faktoren sind, variieren beschrieben in unseren Einreichungen bei der Securities and Exchange Commission.
Informationen zur Telefonkonferenz
CTI-Management wird eine Telefonkonferenz abhalten, um das dritte Quartal Geschäftsjahr 2013 Ergebnisse zu überprüfen und ein Update auf die Geschäftstätigkeit. Die Veranstaltung findet heute um 13.30 Uhr PDT / 16.30 EDT / 9:30 Uhr MEZ werden. Die Teilnehmer können auf den Anruf bei 1-866-225-8754 (USA) oder +1 480-629-9819 (international). Um die Live-Audio-Webcast oder die anschließende archivierte Aufzeichnung zuzugreifen, besuchen Sie CTI-Website, www.celltherapeutics.com . Webcast und Telefon Replays der Telefonkonferenz wird auf etwa zwei Stunden erhalten Sie nach Beendigung des Gesprächs. Anrufer können die Wiedergabe durch Wählen 1-800-406-7325 (USA) oder +1 303-590-3030 (international) zugreifen. Der Zugangscode für die Aufzeichnung lautet 4647208 #. Die telefonische Wiedergabe wird bis Mittwoch, den 6. November 2013 verfügbar sein.
Über Cell Therapeutics, Inc.
Cell Therapeutics (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf den Erwerb, die Entwicklung und Kommerzialisierung von weniger toxisch und effektivere Wege zur Behandlung von Krebs konzentriert. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Non-GAAP-Finanzkennzahlen
CTI hat in dieser Pressemitteilung zur Verfügung gestellt lassen Sie die historischen Finanzinformationen Maß der Verlust aus dem operativen Geschäft, ohne aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, für die neun Monate zum 30. September 2013, und die finanzielle Projektion der Verlust aus dem operativen Geschäft, ohne aktienbasierte Vergütungen, ist das eine nicht GAAP-konforme Kennzahl, für die Geschäftsjahr 2013. Aufgrund unterschiedlicher verfügbar Bewertungsmethoden, subjektiven Annahmen und der verschiedenen GAAP Bilanzierung von verschiedenen award Typen, dass die Unternehmen unter ASC Topic 718 verwenden können, glaubt CTI-Management, dass die Bereitstellung einer Non-GAAP financial measure, die aktienbasierte Vergütung ausschließt kann das Management und der Investoren zu verbessern "Vergleich der Betriebsergebnisse von CTI über verschiedene Zeiträume als den operativen Ergebnissen anderer Unternehmen verglichen.
Unsere Verwendung von Nicht-GAAP financial measure hat seine Grenzen und sollte nicht isoliert von oder als Ersatz für die in Übereinstimmung mit GAAP angesehen werden. Unsere berichtete Non-GAAP-Betriebsergebnis führt zum Ausschluss eines wiederkehrenden Kosten, da aktienbasierte Vergütung wird auch weiterhin eine bedeutende wiederkehrende Aufwendungen in CTI Geschäft sein. Zweitens kann unsere Methodik zur Berechnung des Non-GAAP-Betriebsergebnis, das schließt nur die Komponente der aktienbasierten Vergütung, von der Methodik unserer Peer-Unternehmen zu nutzen, soweit sie berichten Non-GAAP-Verlust aus dem operativen Geschäft oder ähnlich bezeichneten Kennzahlen und dementsprechend unterscheiden nicht unbedingt vergleichbar mit ähnlich bezeichneten Kennzahlen anderer Unternehmen. Anleger werden gebeten, die Vereinbarkeit dieser Non-GAAP-Maßnahmen, um ihre am direktesten vergleichbaren GAAP-Kennzahlen zu überprüfen. Eine Überleitung des CTI Non-GAAP financial measures, um ihre am direktesten vergleichbaren GAAP-Kennzahlen ist in den nachfolgenden Tabellen Jahresrechnung in dieser Pressemitteilung enthaltenen bereitgestellt.
CTI hat noch keine Versöhnung unserer prognostizierten Non-GAAP-Verlust aus dem operativen Geschäft auf eine geplante GAAP-Betriebsverlust enthalten, weil die Berechnung des ausgeschlossenen aktienbasierte Vergütungen Informationen, die derzeit ungewiss ist, wie die künftige Höhe der zusätzlichen Equity Awards erfordern würde, dass gewährt, um CTI Entschädigung Philosophie und Ziele unter Berücksichtigung der Wirtschaftslage zum Zeitpunkt der Gewährung zu erfüllen. Darüber hinaus wird die Berechnung weitgehend auf den Preis des CTI-Aktie zum Zeitpunkt der Gewährung spezifischer Finanzhilfen (wie unter ASC Topic 718 erforderlich), die Preis ist variabel und daher unerkennbar, bis der Zuschuss beruhen. Aufgrund der Zufälligkeit solcher Faktoren, glaubt CTI, dass die spezifische Anpassung für zukünftige aktienbasierte Vergütung kann nicht mit Genauigkeit prognostiziert werden.
Forward-Looking Statements
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, von denen wesentlich und / oder nachteilig auf die tatsächlichen zukünftigen Ergebnisse und den Börsenkurs der CTI Wertpapiere. Solche Aussagen umfassen, sind aber nicht beschränkt auf, Aussagen über CTI die Erwartungen in Bezug auf die Entwicklung von CTI und seine Produkt-und Produkt-Kandidat Portfolio, die Einschreibung für und den Zeitpunkt der PERSIST-2-Studie von pacritinib und CTI die finanzielle Prognose für 2013 wird begrenzt. Risiken, die mit der unsicheren Natur der zukunftsgerichteten Aussagen beitragen, umfassen unter anderem Risiken im Zusammenhang mit der biopharmazeutischen Industrie im Allgemeinen und mit CTI und seine Produkt-und Produkt-Kandidat Portfolio insbesondere auch, unter anderem, Risiken im Zusammenhang mit der folgenden assoziiert: dass CTI kann nicht vorhersagen oder garantieren das Tempo oder Geographie der Einschreibung ihrer klinischen Studien; die CTI können nicht vorhersagen oder Garantie für die Ergebnisse der vorklinischen und klinischen Studien; die CTI können keine Rückerstattung für Pixuvri in bestimmten Märkten in der EU wie geplant oder überhaupt; dass die bedingte Zulassung von Pixuvri kann nicht verlängert werden oder kann zusätzlichen Bedingungen unterliegen, dass die PERSIST-2-Studie von pacritinib wird nicht auftreten, wie geplant oder überhaupt; dass CTI nicht gestattet günstigen Bestimmungen durch andere Regulierungs-, Patent-und Verwaltungsvorschriften Regierungsbehörden; Risiken im Zusammenhang mit den Kosten für die Entwicklung, Herstellung und Verkauf Pixuvri pacritinib und CTI anderen Produkt-Kandidaten;; dass CTI können Verzögerungen bei Beginn der präklinischen und klinischen Studien zu erleben und andere Risiken, einschließlich, ohne Einschränkung, Wettbewerbsfaktoren, technologische Entwicklungen, dass CTI die Betriebskosten, die Netto-Einnahmen nicht übersteigen weiterhin, dass CTI nicht in der Lage, seine aktuellen Kostenkontrolle erhalten oder weiter zu verringern die Betriebskosten, die CTI nicht erreichen angekündigten Ziele wie oder bei der Projektion, dass CTI durchschnittliche operative Netto-Burn-Rate erhöhen, dass CTI weiterhin brauchen, um Kapital aufzubringen, um die Betriebskosten zu finanzieren, kann aber nicht in der Lage sein, ausreichende Mengen an deren weiterem Betrieb zu finanzieren, sowie andere Risiken, die aufgelistet oder von Zeit zu Zeit beschrieben erhöhen CTI in den neuesten Einreichungen bei der Securities and Exchange Commission auf den Formularen 10-K, 10-Q und 8-K. Sofern nicht gesetzlich vorgeschrieben, übernimmt CTI nicht die Absicht, eine der Aussagen in dieser Pressemitteilung auf weitere Entwicklungen zu aktualisieren.
Pixuvri ist ein eingetragenes Warenzeichen von Cell Therapeutics, Inc.
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206-282-7100
ebell@ctiseattle.com
In Europa:
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
+39 02 89659706
lvilla@cti-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
http://finance.yahoo.com/news/...reports-third-quarter-200000798.html
SEATTLE, 30. Oktober 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute die Finanzergebnisse für das dritte Quartal und die neun Monate zum 30. September 2013 bestellen.
"Wir haben vor kurzem erreicht einen wichtigen klinischen Meilenstein in unserer Entwicklung pacritinib Programm, nachdem eine Einigung mit der FDA auf einem Special Protocol Assessment (SPA) für die geplante Phase-3-PERSIST-2-Studie von pacritinib für Patienten mit Myelofibrose, die niedrige Thrombozyten haben ", sagte James Bianco, MD, Präsident und CEO von CTI. "Mit der SPA im Ort, erwarten wir, diese Studie im vierten Quartal 2013 zu initiieren und zu antizipieren Abschluss Einschreibung in etwa 12 Monaten. Wir weiterhin Fortschritte bei der Erstattung Verfahren zur PIXVURI in der Europäischen Union zu machen und sind auf Fortbildung von Ärzten, konzentrierte sich auf die nicht gedeckten medizinischen Bedarf und Gebäude Markenbekanntheit für Pixuvri als dritten und vierten-Line-Behandlung Option unter den Ärzten in Ländern, in denen Pixuvri derzeit verfügbar ist. "
Drittes Quartal 2013 sowie Schlagzeilen
Pixuvri ® (pixantrone) Commercial: Market Access in Frankreich und Italien gewährt
Berichtet, dass das Unternehmen den Marktzugang wurde von der Kommission Transparenz des Französisch National Health Authority in Frankreich und von der italienischen Arzneimittelbehörde (AIFA) in Italien für Pixuvri gewährt als Monotherapie zur Behandlung von erwachsenen Patienten mit mehrfach rezidivierten oder refraktären aggressiven B- Zell-NHL (Patienten mit aggressiven B-Zell-NHL, die 2 oder 3 vorherige Behandlungen fehlgeschlagen).
Forschung und Entwicklung: Erreichte SPA-Abkommen mit FDA für PERSIST-2 Clinical Trial
Einigung mit der US Food and Drug Administration (FDA) auf einem SPA für die geplante Phase-3-Studie, als PERSIST-2 bekannt, Auswertung pacritinib Vergleich zum besten verfügbaren Therapie, einschließlich genehmigt JAK2-Inhibitoren wie ruxolitinib, bei Patienten mit Myelofibrose deren Blutplättchen sind
Firmenintern: Expanded CTI des Wissenschaftlichen Beirats und angehoben Etwa 15 Millionen Dollar Finanzierung.
Hinzugefügt drei Staats-und Regierungschefs in der Forschung und Entwicklung von neuen Therapien für Blut-Krebsarten vor kurzem gebildet Scientific CTI Advisory Board (SAB): Alan List, MD, Präsident und CEO von Moffitt Cancer Center; Ross Levine, MD, Associate Oberarzt am Memorial Sloan-Kettering Cancer Center, und Brian Druker, MD, Direktor des Ritters Cancer Institute an der Oregon Health & Science University. CTI SAB wird von Daniel Von Hoff, MD, BMZ Vorsitz
Abgeschlossen eingetragenen direkten Angebot ohne Underwriter oder Placement Agent für Nettoerlös von rund $ 14.800.000.
Third Quarter 2013 Financial Results
Der Gesamtumsatz für das dritte Quartal und die ersten neun Monate zum 30. September 2013 waren 0.400.000 $ und $ 1,8 Mio. bzw.. Die Einnahmen waren ausschließlich auf Netto-Produktverkäufe von Pixuvri. CTI Pixuvri verkauft direkt an Anbietern von Gesundheitsleistungen und durch eine begrenzte Zahl von Großhändlern in der EU im Allgemeinen zeichnet CTI Produktverkäufe nach Erhalt der Ware durch den Arzt oder Vertreiber, abzüglich Händler Rabatte, geschätzt staatlich verordneten Preisnachlässe und Rabatte, und geschätzte Retouren. Alle künftigen Einnahmen sind abhängig von der Marktakzeptanz Pixuvri, die Entscheidungen über Erstattung von staatlichen Behörden in jedem Land, in dem Pixuvri steht zum Verkauf und andere Faktoren gemacht.
Der operative Verlust für das dritte Quartal 2013 betrug $ 15,6 Mio. im Vergleich zu $ 15.100.000 für den gleichen Zeitraum im Jahr 2012. Für die ersten neun Monate des Jahres 2013 war der operative Verlust $ 51.900.000 gegenüber $ 82.600.000 für den gleichen Zeitraum im Jahr 2012. Der Betrag für die neun Monate zum 30. September aufgezeichnet, inklusive 2012 ein $ 29.100.000 Aufwendungen für erworbene in Arbeit befindliche Forschung und Entwicklung im Zusammenhang mit dem Erwerb von pacritinib von S * BIO Pte Ltd Non-cash, aktienbasierte Vergütungen beliefen sich im dritten Quartal und die ersten neun Monate 2013 betrug $ 1.900.000 und $ 6,3 Mio., verglichen zu $ 1,0 Mio. und $ 6.100.000 für den gleichen Zeitraum im Jahr 2012.
Der Nettoverlust für das dritte Quartal 2013 war $ 22.400.000 oder ($ 0.20) pro Aktie, verglichen mit $ 20.200.000 oder ($ 0,38) je Aktie für den gleichen Zeitraum im Jahr 2012. Für die ersten neun Monate des Jahres 2013, war Nettoverlust $ 59.800.000 oder ($ 0,55) pro Aktie, verglichen mit $ 96.200.000 oder ($ 2.12) pro Aktie für den gleichen Zeitraum im Jahr 2012.
Zum 30. September 2013, betrug CTI Zahlungsmittel und Zahlungsmitteläquivalente $ 27.200.000.
Finanzprognose für das Jahr 2013
CTI bekräftigt vor finanzielle Führung, dass für das Jahr 2013, Betriebsergebnis abzüglich unbare, aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, wird erwartet, dass rund $ 60 bis $ 65.000.000 zu sein. Year-to-date für die ersten neun Monate zum 30. September 2013, des Betriebsergebnisses, ohne nicht zahlungswirksame aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, war $ 45.500.000. Für weitere Informationen über CTI Verwendung dieser nicht GAAP-konformen Kennzahlen und eine Überleitung Non-GAAP-Betriebsergebnis abzüglich unbare aktienbasierte Vergütungen, um den Verlust aus dem operativen Geschäft für die neun Monate zum 30. September 2013, finden Sie im Abschnitt unter dem Titel "Non-GAAP-konformen Finanzkennzahlen".
Tatsächlichen finanziellen Ergebnisse für das Jahr 2013 wird von vielen Faktoren ab, einschließlich des Grades der Marktakzeptanz und Bestimmung der Erstattungssätze für Pixuvri in der EU, die Rate der Patientenrekrutierung in klinischen Studien, die pacritinib laufenden und geplanten für die Initiierung im Jahr 2013 und andere Faktoren sind, variieren beschrieben in unseren Einreichungen bei der Securities and Exchange Commission.
Informationen zur Telefonkonferenz
CTI-Management wird eine Telefonkonferenz abhalten, um das dritte Quartal Geschäftsjahr 2013 Ergebnisse zu überprüfen und ein Update auf die Geschäftstätigkeit. Die Veranstaltung findet heute um 13.30 Uhr PDT / 16.30 EDT / 9:30 Uhr MEZ werden. Die Teilnehmer können auf den Anruf bei 1-866-225-8754 (USA) oder +1 480-629-9819 (international). Um die Live-Audio-Webcast oder die anschließende archivierte Aufzeichnung zuzugreifen, besuchen Sie CTI-Website, www.celltherapeutics.com . Webcast und Telefon Replays der Telefonkonferenz wird auf etwa zwei Stunden erhalten Sie nach Beendigung des Gesprächs. Anrufer können die Wiedergabe durch Wählen 1-800-406-7325 (USA) oder +1 303-590-3030 (international) zugreifen. Der Zugangscode für die Aufzeichnung lautet 4647208 #. Die telefonische Wiedergabe wird bis Mittwoch, den 6. November 2013 verfügbar sein.
Über Cell Therapeutics, Inc.
Cell Therapeutics (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf den Erwerb, die Entwicklung und Kommerzialisierung von weniger toxisch und effektivere Wege zur Behandlung von Krebs konzentriert. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Non-GAAP-Finanzkennzahlen
CTI hat in dieser Pressemitteilung zur Verfügung gestellt lassen Sie die historischen Finanzinformationen Maß der Verlust aus dem operativen Geschäft, ohne aktienbasierte Vergütungen, die eine nicht GAAP-konforme Kennzahl ist, für die neun Monate zum 30. September 2013, und die finanzielle Projektion der Verlust aus dem operativen Geschäft, ohne aktienbasierte Vergütungen, ist das eine nicht GAAP-konforme Kennzahl, für die Geschäftsjahr 2013. Aufgrund unterschiedlicher verfügbar Bewertungsmethoden, subjektiven Annahmen und der verschiedenen GAAP Bilanzierung von verschiedenen award Typen, dass die Unternehmen unter ASC Topic 718 verwenden können, glaubt CTI-Management, dass die Bereitstellung einer Non-GAAP financial measure, die aktienbasierte Vergütung ausschließt kann das Management und der Investoren zu verbessern "Vergleich der Betriebsergebnisse von CTI über verschiedene Zeiträume als den operativen Ergebnissen anderer Unternehmen verglichen.
Unsere Verwendung von Nicht-GAAP financial measure hat seine Grenzen und sollte nicht isoliert von oder als Ersatz für die in Übereinstimmung mit GAAP angesehen werden. Unsere berichtete Non-GAAP-Betriebsergebnis führt zum Ausschluss eines wiederkehrenden Kosten, da aktienbasierte Vergütung wird auch weiterhin eine bedeutende wiederkehrende Aufwendungen in CTI Geschäft sein. Zweitens kann unsere Methodik zur Berechnung des Non-GAAP-Betriebsergebnis, das schließt nur die Komponente der aktienbasierten Vergütung, von der Methodik unserer Peer-Unternehmen zu nutzen, soweit sie berichten Non-GAAP-Verlust aus dem operativen Geschäft oder ähnlich bezeichneten Kennzahlen und dementsprechend unterscheiden nicht unbedingt vergleichbar mit ähnlich bezeichneten Kennzahlen anderer Unternehmen. Anleger werden gebeten, die Vereinbarkeit dieser Non-GAAP-Maßnahmen, um ihre am direktesten vergleichbaren GAAP-Kennzahlen zu überprüfen. Eine Überleitung des CTI Non-GAAP financial measures, um ihre am direktesten vergleichbaren GAAP-Kennzahlen ist in den nachfolgenden Tabellen Jahresrechnung in dieser Pressemitteilung enthaltenen bereitgestellt.
CTI hat noch keine Versöhnung unserer prognostizierten Non-GAAP-Verlust aus dem operativen Geschäft auf eine geplante GAAP-Betriebsverlust enthalten, weil die Berechnung des ausgeschlossenen aktienbasierte Vergütungen Informationen, die derzeit ungewiss ist, wie die künftige Höhe der zusätzlichen Equity Awards erfordern würde, dass gewährt, um CTI Entschädigung Philosophie und Ziele unter Berücksichtigung der Wirtschaftslage zum Zeitpunkt der Gewährung zu erfüllen. Darüber hinaus wird die Berechnung weitgehend auf den Preis des CTI-Aktie zum Zeitpunkt der Gewährung spezifischer Finanzhilfen (wie unter ASC Topic 718 erforderlich), die Preis ist variabel und daher unerkennbar, bis der Zuschuss beruhen. Aufgrund der Zufälligkeit solcher Faktoren, glaubt CTI, dass die spezifische Anpassung für zukünftige aktienbasierte Vergütung kann nicht mit Genauigkeit prognostiziert werden.
Forward-Looking Statements
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, von denen wesentlich und / oder nachteilig auf die tatsächlichen zukünftigen Ergebnisse und den Börsenkurs der CTI Wertpapiere. Solche Aussagen umfassen, sind aber nicht beschränkt auf, Aussagen über CTI die Erwartungen in Bezug auf die Entwicklung von CTI und seine Produkt-und Produkt-Kandidat Portfolio, die Einschreibung für und den Zeitpunkt der PERSIST-2-Studie von pacritinib und CTI die finanzielle Prognose für 2013 wird begrenzt. Risiken, die mit der unsicheren Natur der zukunftsgerichteten Aussagen beitragen, umfassen unter anderem Risiken im Zusammenhang mit der biopharmazeutischen Industrie im Allgemeinen und mit CTI und seine Produkt-und Produkt-Kandidat Portfolio insbesondere auch, unter anderem, Risiken im Zusammenhang mit der folgenden assoziiert: dass CTI kann nicht vorhersagen oder garantieren das Tempo oder Geographie der Einschreibung ihrer klinischen Studien; die CTI können nicht vorhersagen oder Garantie für die Ergebnisse der vorklinischen und klinischen Studien; die CTI können keine Rückerstattung für Pixuvri in bestimmten Märkten in der EU wie geplant oder überhaupt; dass die bedingte Zulassung von Pixuvri kann nicht verlängert werden oder kann zusätzlichen Bedingungen unterliegen, dass die PERSIST-2-Studie von pacritinib wird nicht auftreten, wie geplant oder überhaupt; dass CTI nicht gestattet günstigen Bestimmungen durch andere Regulierungs-, Patent-und Verwaltungsvorschriften Regierungsbehörden; Risiken im Zusammenhang mit den Kosten für die Entwicklung, Herstellung und Verkauf Pixuvri pacritinib und CTI anderen Produkt-Kandidaten;; dass CTI können Verzögerungen bei Beginn der präklinischen und klinischen Studien zu erleben und andere Risiken, einschließlich, ohne Einschränkung, Wettbewerbsfaktoren, technologische Entwicklungen, dass CTI die Betriebskosten, die Netto-Einnahmen nicht übersteigen weiterhin, dass CTI nicht in der Lage, seine aktuellen Kostenkontrolle erhalten oder weiter zu verringern die Betriebskosten, die CTI nicht erreichen angekündigten Ziele wie oder bei der Projektion, dass CTI durchschnittliche operative Netto-Burn-Rate erhöhen, dass CTI weiterhin brauchen, um Kapital aufzubringen, um die Betriebskosten zu finanzieren, kann aber nicht in der Lage sein, ausreichende Mengen an deren weiterem Betrieb zu finanzieren, sowie andere Risiken, die aufgelistet oder von Zeit zu Zeit beschrieben erhöhen CTI in den neuesten Einreichungen bei der Securities and Exchange Commission auf den Formularen 10-K, 10-Q und 8-K. Sofern nicht gesetzlich vorgeschrieben, übernimmt CTI nicht die Absicht, eine der Aussagen in dieser Pressemitteilung auf weitere Entwicklungen zu aktualisieren.
Pixuvri ist ein eingetragenes Warenzeichen von Cell Therapeutics, Inc.
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206-282-7100
ebell@ctiseattle.com
In Europa:
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
+39 02 89659706
lvilla@cti-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
15.11.13 16:58
#930
Heron
strategische Zusammenarbeit mit Baxter
Baxter und Cell Therapeutics kündigt weltweite strategische Zusammenarbeit zur Entwicklung und Vermarktung Pacritinib
Pacritinib zulassungsrelevanten klinischen Phase III-Programm für Myelofibrosis Under Way
Business Wire
Baxter International Inc. vor 3 Stunden
http://finance.yahoo.com/news/...cs-announce-worldwide-123000574.html
Deerfield, Illinois & SEATTLE - (BUSINESS WIRE) -
Baxter International Inc. ( BAX ) und Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) haben heute gemeinsam bekannt, dass sie eine exklusive weltweite Lizenzvereinbarung zur Entwicklung und Kommerzialisierung pacritinib eingetragen. Pacritinib ist ein neuartiger JAK2/FLT3 Inhibitor mit Aktivität gegen genetische Mutationen in Verbindung mit Myelofibrose, Leukämie und bestimmten soliden Tumoren. Pacritinib befindet sich derzeit in Phase III der klinischen Entwicklung für Patienten mit Myelofibrose, einer chronischen malignen Erkrankung des Knochenmarks.
Gemäß den Bedingungen der Vereinbarung erhält Baxter exklusiven Vermarktungsrechte für alle Indikationen für pacritinib außerhalb der Vereinigten Staaten und Baxter und CTI gemeinsam vermarkten pacritinib in den Vereinigten Staaten. Baxter wird eine Vorauszahlung in Höhe von 60 Millionen Dollar, die eine Beteiligung an der CTI 30 Millionen Dollar umfasst. Darüber hinaus ist CTI berechtigt, klinischer, regulatorischer und Markteinführung Meilensteinzahlungen von bis zu 112.000.000 $, $ 40 Mio., wovon die klinische Meilensteine, die im Jahr 2014 erreicht werden kann bezieht erhalten. Unter der Annahme, Zulassung und Markteinführung kann CTI erhalten zusätzliche Umsätze Meilenstein-Zahlungen. CTI wird Lizenzgebühren auf den Nettoumsatz von pacritinib in ex-US Märkte zu erhalten, und die Unternehmen werden US Gewinne zu gleichen Teilen. Baxter zeichnet eine besondere Vorsteuerergebnis in-process Forschung und Entwicklung Ladung im vierten Quartal 2013 von rund USD 30 Millionen Euro.
'' Die Zusammenarbeit ergänzen Baxter bestehenden Geschäftsfeld Onkologie und wachsenden Onkologie-Pipeline, und werden unsere weltweite Vermarktung Kapazität, um die Verfügbarkeit von pacritinib, die wir glauben, hat das Potenzial, einen erheblichen ungedeckten medizinischen Bedarf zu verlängern'', sagte Ludwig Hantson, Ph . D., Präsident von Baxter BioScience. '' Als etablierter Marktführer in der Hämatologie und seltene Krankheiten, sind wir für die Weiterentwicklung neuartiger Therapien in dem Bemühen, den Zugang der Patienten zu kümmern erweitern begangen.''
'' Wir glauben, Baxter stellt den idealen strategischen Partner, um das volle Potenzial der pacritinib erreichen'', sagte James A. Bianco, MD, Präsident und CEO von CTI. '' Unsere beiden Unternehmen teilen sich ein Engagement in der Onkologie und eine Vision für die Erhebung dieser einmaligen oralen JAK2/FLT3 Hemmstoff, um Patienten mit bestimmten Blutkrebs und soliden Tumoren. Diese Zusammenarbeit wird zusätzliche finanzielle Ressourcen und kaufmännisches Know-how, um uns zu positionieren, um die Entwicklung, Kommerzialisierung und Marktpotenzial von pacritinib verfolgen.''
Pacritinib ist ein oraler Tyrosinkinase-Inhibitor (TKI) mit Dual-Aktivität gegen JAK2 und FLT3. Die JAK-Familie von Enzymen ist ein zentraler Bestandteil in Signaltransduktionswegen, die entscheidend für die normale Blutkörperchen Wachstum und Entwicklung sowie entzündlichen Zytokin-Expression und Immunreaktionen sind. Mutationen in diesen Kinasen haben gezeigt, dass direkt an der Entwicklung bestimmter Krebsarten einschließlich Blut myeloproliferativen Neoplasien, Leukämie und Lymphom bezogen werden.
Über die Phase-III-Programm Pacritinib
Ergebnisse aus früheren Phase-I-und-II-Studien von pacritinib zeigte ermutigende Ergebnisse, einschließlich aussagekräftige klinische Vorteile bei guter Verträglichkeit bei Patienten mit fortgeschrittener Myelofibrose gekoppelt. Basierend auf der Wirksamkeit und Verträglichkeit nachgewiesen to date enthält das zentrale Programm zur pacritinib zwei Phase-III-Studien: PERSIST-1 ist die Untersuchung der Wirksamkeit und Sicherheit in einem breiten Spektrum von Patienten mit Myelofibrose ohne Einschränkungen auf Blutplättchen und PERSIST-2 wird die Wirksamkeit und Sicherheit bei Patienten mit niedrigen Thrombozytenzahlen bewerten, und wird voraussichtlich im vierten Quartal 2013 beginnen.
Über Baxter in der Onkologie
Baxter setzt sein Portfolio an Markenprodukten und F & E-Programme in der Onkologie zu erweitern. Aktuelle Produkte umfassen Chemotherapeutika allein oder in Kombination mit anderen Produkten verwendet werden, um Krebserkrankungen wie Non-Hodgkin-Lymphom, sowie Anti-Brechmittel Produkte entwickelt, um die Nebenwirkungen der Krebstherapie lindern. Aktuelle Kooperationen und Entwicklungsprogramme haben weitere Baxter Fußabdruck in der Hämatologie / Onkologie erweitert, aufbauend auf die Kompetenz des Unternehmens in der Behandlung von Patienten mit lebensbedrohlichen Erkrankungen.
Über Baxter International Inc.
Baxter International Inc. und ihre Tochtergesellschaften, entwickelt, produziert und vertreibt Produkte, die das Leben von Menschen mit Hämophilie, Immunerkrankungen, Krebs, Infektionskrankheiten, Nierenerkrankungen, Traumata und anderen chronischen und akuten Erkrankungen. Als globales, diversifiziertes Gesundheitsunternehmen verbindet Baxter seine Expertise in medizinischen Geräten, Pharmazeutika und Biotechnologie, um Produkte, welche die Patientenversorgung weltweit zu schaffen.
Über Cell Therapeutics
Cell Therapeutics Inc. (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen in Bezug auf eine Kooperationsvereinbarung zwischen Baxter International Inc. und Cell Therapeutics Inc., die im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995 sind. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, welche sich wesentlich und / oder nachteilig auf tatsächliche zukünftige Ergebnisse und der Börsenkurs der Wertpapiere der Emittenten. Solche Aussagen umfassen, sind jedoch nicht darauf beschränkt, Erwartungen in Bezug auf Meilenstein-und Lizenzzahlungen, die erwartete Vorteile der Zusammenarbeit und der Fähigkeit, das Potenzial pacritinib maximieren und Erweiterung der Anwendbarkeit auf andere Tumoren, einschließlich Tumoren. Die Aussagen beruhen auf Annahmen hinsichtlich zahlreicher wichtiger Faktoren, einschließlich der folgenden, aufgrund derer die tatsächlichen Ergebnisse wesentlich von jenen abweichen, die in den zukunftsgerichteten Aussagen getätigt wurden, basieren:; Maßnahmen der Regulierungsbehörden und anderen staatlichen Behörden, die Zufriedenheit der Regulierungs-und anderen Anforderungen klinischen Studie Ergebnisse, Änderungen in Gesetzen und Vorschriften; Produktqualität oder Fragen der Patientensicherheit; Risiken der Produktentwicklung, die Auswirkungen von wettbewerbsfähigen Produkten und Preisgestaltung und Kostenerstattung, sowie andere Risiken in einzelnen Emittenten in den neuesten Einreichungen auf Formular 10-K und anderen Securities and Exchange Commission Einreichungen. Weder Baxter noch CTI verpflichtet sich, seine zukunftsgerichteten Aussagen zu aktualisieren.
Fotos / Multimedia-Galerie verfügbar unter: http://www.businesswire.com/multimedia/home/20131115005117/en/
MULTIMEDIA VERFÜGBAR: http://www.businesswire.com/cgi-bin/mmg.cgi?eid=50751770&lang=en
Kontakt:
Baxter Media Contacts
Brian Kyhos oder Deborah Spak
(224) 948-5353
media@baxter.com
oder
Baxter Investor Kontakt
Mary Kay LaDone, (224) 948-3371
oder
CTI Kontakt
Monique Greer
206-272-4343
mgreer@ctiseattle.com
Pacritinib zulassungsrelevanten klinischen Phase III-Programm für Myelofibrosis Under Way
Business Wire
Baxter International Inc. vor 3 Stunden
http://finance.yahoo.com/news/...cs-announce-worldwide-123000574.html
Deerfield, Illinois & SEATTLE - (BUSINESS WIRE) -
Baxter International Inc. ( BAX ) und Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) haben heute gemeinsam bekannt, dass sie eine exklusive weltweite Lizenzvereinbarung zur Entwicklung und Kommerzialisierung pacritinib eingetragen. Pacritinib ist ein neuartiger JAK2/FLT3 Inhibitor mit Aktivität gegen genetische Mutationen in Verbindung mit Myelofibrose, Leukämie und bestimmten soliden Tumoren. Pacritinib befindet sich derzeit in Phase III der klinischen Entwicklung für Patienten mit Myelofibrose, einer chronischen malignen Erkrankung des Knochenmarks.
Gemäß den Bedingungen der Vereinbarung erhält Baxter exklusiven Vermarktungsrechte für alle Indikationen für pacritinib außerhalb der Vereinigten Staaten und Baxter und CTI gemeinsam vermarkten pacritinib in den Vereinigten Staaten. Baxter wird eine Vorauszahlung in Höhe von 60 Millionen Dollar, die eine Beteiligung an der CTI 30 Millionen Dollar umfasst. Darüber hinaus ist CTI berechtigt, klinischer, regulatorischer und Markteinführung Meilensteinzahlungen von bis zu 112.000.000 $, $ 40 Mio., wovon die klinische Meilensteine, die im Jahr 2014 erreicht werden kann bezieht erhalten. Unter der Annahme, Zulassung und Markteinführung kann CTI erhalten zusätzliche Umsätze Meilenstein-Zahlungen. CTI wird Lizenzgebühren auf den Nettoumsatz von pacritinib in ex-US Märkte zu erhalten, und die Unternehmen werden US Gewinne zu gleichen Teilen. Baxter zeichnet eine besondere Vorsteuerergebnis in-process Forschung und Entwicklung Ladung im vierten Quartal 2013 von rund USD 30 Millionen Euro.
'' Die Zusammenarbeit ergänzen Baxter bestehenden Geschäftsfeld Onkologie und wachsenden Onkologie-Pipeline, und werden unsere weltweite Vermarktung Kapazität, um die Verfügbarkeit von pacritinib, die wir glauben, hat das Potenzial, einen erheblichen ungedeckten medizinischen Bedarf zu verlängern'', sagte Ludwig Hantson, Ph . D., Präsident von Baxter BioScience. '' Als etablierter Marktführer in der Hämatologie und seltene Krankheiten, sind wir für die Weiterentwicklung neuartiger Therapien in dem Bemühen, den Zugang der Patienten zu kümmern erweitern begangen.''
'' Wir glauben, Baxter stellt den idealen strategischen Partner, um das volle Potenzial der pacritinib erreichen'', sagte James A. Bianco, MD, Präsident und CEO von CTI. '' Unsere beiden Unternehmen teilen sich ein Engagement in der Onkologie und eine Vision für die Erhebung dieser einmaligen oralen JAK2/FLT3 Hemmstoff, um Patienten mit bestimmten Blutkrebs und soliden Tumoren. Diese Zusammenarbeit wird zusätzliche finanzielle Ressourcen und kaufmännisches Know-how, um uns zu positionieren, um die Entwicklung, Kommerzialisierung und Marktpotenzial von pacritinib verfolgen.''
Pacritinib ist ein oraler Tyrosinkinase-Inhibitor (TKI) mit Dual-Aktivität gegen JAK2 und FLT3. Die JAK-Familie von Enzymen ist ein zentraler Bestandteil in Signaltransduktionswegen, die entscheidend für die normale Blutkörperchen Wachstum und Entwicklung sowie entzündlichen Zytokin-Expression und Immunreaktionen sind. Mutationen in diesen Kinasen haben gezeigt, dass direkt an der Entwicklung bestimmter Krebsarten einschließlich Blut myeloproliferativen Neoplasien, Leukämie und Lymphom bezogen werden.
Über die Phase-III-Programm Pacritinib
Ergebnisse aus früheren Phase-I-und-II-Studien von pacritinib zeigte ermutigende Ergebnisse, einschließlich aussagekräftige klinische Vorteile bei guter Verträglichkeit bei Patienten mit fortgeschrittener Myelofibrose gekoppelt. Basierend auf der Wirksamkeit und Verträglichkeit nachgewiesen to date enthält das zentrale Programm zur pacritinib zwei Phase-III-Studien: PERSIST-1 ist die Untersuchung der Wirksamkeit und Sicherheit in einem breiten Spektrum von Patienten mit Myelofibrose ohne Einschränkungen auf Blutplättchen und PERSIST-2 wird die Wirksamkeit und Sicherheit bei Patienten mit niedrigen Thrombozytenzahlen bewerten, und wird voraussichtlich im vierten Quartal 2013 beginnen.
Über Baxter in der Onkologie
Baxter setzt sein Portfolio an Markenprodukten und F & E-Programme in der Onkologie zu erweitern. Aktuelle Produkte umfassen Chemotherapeutika allein oder in Kombination mit anderen Produkten verwendet werden, um Krebserkrankungen wie Non-Hodgkin-Lymphom, sowie Anti-Brechmittel Produkte entwickelt, um die Nebenwirkungen der Krebstherapie lindern. Aktuelle Kooperationen und Entwicklungsprogramme haben weitere Baxter Fußabdruck in der Hämatologie / Onkologie erweitert, aufbauend auf die Kompetenz des Unternehmens in der Behandlung von Patienten mit lebensbedrohlichen Erkrankungen.
Über Baxter International Inc.
Baxter International Inc. und ihre Tochtergesellschaften, entwickelt, produziert und vertreibt Produkte, die das Leben von Menschen mit Hämophilie, Immunerkrankungen, Krebs, Infektionskrankheiten, Nierenerkrankungen, Traumata und anderen chronischen und akuten Erkrankungen. Als globales, diversifiziertes Gesundheitsunternehmen verbindet Baxter seine Expertise in medizinischen Geräten, Pharmazeutika und Biotechnologie, um Produkte, welche die Patientenversorgung weltweit zu schaffen.
Über Cell Therapeutics
Cell Therapeutics Inc. (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI ist in Seattle, WA ansässig. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte www.CellTherapeutics.com .
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen in Bezug auf eine Kooperationsvereinbarung zwischen Baxter International Inc. und Cell Therapeutics Inc., die im Sinne der Safe-Harbor-Bestimmungen des Private Securities Litigation Reform Act von 1995 sind. Solche Aussagen unterliegen einer Reihe von Risiken und Unabwägbarkeiten beinhalten, welche sich wesentlich und / oder nachteilig auf tatsächliche zukünftige Ergebnisse und der Börsenkurs der Wertpapiere der Emittenten. Solche Aussagen umfassen, sind jedoch nicht darauf beschränkt, Erwartungen in Bezug auf Meilenstein-und Lizenzzahlungen, die erwartete Vorteile der Zusammenarbeit und der Fähigkeit, das Potenzial pacritinib maximieren und Erweiterung der Anwendbarkeit auf andere Tumoren, einschließlich Tumoren. Die Aussagen beruhen auf Annahmen hinsichtlich zahlreicher wichtiger Faktoren, einschließlich der folgenden, aufgrund derer die tatsächlichen Ergebnisse wesentlich von jenen abweichen, die in den zukunftsgerichteten Aussagen getätigt wurden, basieren:; Maßnahmen der Regulierungsbehörden und anderen staatlichen Behörden, die Zufriedenheit der Regulierungs-und anderen Anforderungen klinischen Studie Ergebnisse, Änderungen in Gesetzen und Vorschriften; Produktqualität oder Fragen der Patientensicherheit; Risiken der Produktentwicklung, die Auswirkungen von wettbewerbsfähigen Produkten und Preisgestaltung und Kostenerstattung, sowie andere Risiken in einzelnen Emittenten in den neuesten Einreichungen auf Formular 10-K und anderen Securities and Exchange Commission Einreichungen. Weder Baxter noch CTI verpflichtet sich, seine zukunftsgerichteten Aussagen zu aktualisieren.
Fotos / Multimedia-Galerie verfügbar unter: http://www.businesswire.com/multimedia/home/20131115005117/en/
MULTIMEDIA VERFÜGBAR: http://www.businesswire.com/cgi-bin/mmg.cgi?eid=50751770&lang=en
Kontakt:
Baxter Media Contacts
Brian Kyhos oder Deborah Spak
(224) 948-5353
media@baxter.com
oder
Baxter Investor Kontakt
Mary Kay LaDone, (224) 948-3371
oder
CTI Kontakt
Monique Greer
206-272-4343
mgreer@ctiseattle.com
15.11.13 17:04
#931
Heron
Telefonkonferenz Heute
Cell Therapeutics kündigt Telefonkonferenz Heute, Freitag, 15. November 2013 um 8:30 Uhr Eastern Time bewirten, um Pacritinib Partnership Diskutieren
13.40 15.11.13
PR Newswire
SEATTLE, 15. November 2013
http://www.ariva.de/news/...to-Discuss-Pacritinib-Partnership-4847546
SEATTLE, November 15, 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute bekannt, dass die Mitglieder des Managements eine Telefonkonferenz veranstalten heute, Freitag, 15. November 2013 um 8:30 Uhr ET (5 : 30 Uhr PT) der heutigen Ankündigung in Bezug auf die weltweite Lizenzvereinbarung zwischen Baxter International, Inc. und CTI zu entwickeln und zu kommerzialisieren pacritinib, CTI neuartiger JAK2/FLT3 Inhibitor derzeit in Phase-3-Entwicklung für Patienten mit Myelofibrose diskutieren. Der Zugang zu der Veranstaltung kann wie folgt erhalten werden:
FREITAG November, 15. Mai 2013
05.30 PT / 08.30 Uhr ET / 14.30 Uhr CET
1-800-762 - 8779 (Inland)
+1 480-629-9645 (international)
Um die Live-Audio-Webcast oder die anschließende archivierte Aufzeichnung zuzugreifen, besuchen www.celltherapeutics.com . Webcast und Telefon Replays der Telefonkonferenz wird auf etwa zwei Stunden erhalten Sie nach Beendigung des Gesprächs. Anrufer können die Wiedergabe durch Wählen 1-800-406-7325 (USA) oder +1 303-590-3030 (international) zugreifen. Der Zugangscode für die Aufzeichnung lautet 4651503. Die telefonische Wiedergabe wird bis zum Freitag, 22. November 2013 verfügbar sein.
Über Cell Therapeutics, Inc.
Cell Therapeutics (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI in Seattle, WA Hauptsitz. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte die Website des Unternehmens auf www.CellTherapeutics.com .
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206.282.7100
ebell@ctiseattle.com
In Europa
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
T: +39 02 89659706
E: lvilla @ CTI-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
SOURCE Cell Therapeutics, Inc.
Quelle: PR Newswire
13.40 15.11.13
PR Newswire
SEATTLE, 15. November 2013
http://www.ariva.de/news/...to-Discuss-Pacritinib-Partnership-4847546
SEATTLE, November 15, 2013 / PRNewswire / - Cell Therapeutics, Inc. (CTI) (NASDAQ und MTA: CTIC) gab heute bekannt, dass die Mitglieder des Managements eine Telefonkonferenz veranstalten heute, Freitag, 15. November 2013 um 8:30 Uhr ET (5 : 30 Uhr PT) der heutigen Ankündigung in Bezug auf die weltweite Lizenzvereinbarung zwischen Baxter International, Inc. und CTI zu entwickeln und zu kommerzialisieren pacritinib, CTI neuartiger JAK2/FLT3 Inhibitor derzeit in Phase-3-Entwicklung für Patienten mit Myelofibrose diskutieren. Der Zugang zu der Veranstaltung kann wie folgt erhalten werden:
FREITAG November, 15. Mai 2013
05.30 PT / 08.30 Uhr ET / 14.30 Uhr CET
1-800-762 - 8779 (Inland)
+1 480-629-9645 (international)
Um die Live-Audio-Webcast oder die anschließende archivierte Aufzeichnung zuzugreifen, besuchen www.celltherapeutics.com . Webcast und Telefon Replays der Telefonkonferenz wird auf etwa zwei Stunden erhalten Sie nach Beendigung des Gesprächs. Anrufer können die Wiedergabe durch Wählen 1-800-406-7325 (USA) oder +1 303-590-3030 (international) zugreifen. Der Zugangscode für die Aufzeichnung lautet 4651503. Die telefonische Wiedergabe wird bis zum Freitag, 22. November 2013 verfügbar sein.
Über Cell Therapeutics, Inc.
Cell Therapeutics (NASDAQ und MTA: CTIC) ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung eines integrierten Portfolios onkologischer Produkte für eine erfolgreichere Krebsbehandlung verschrieben hat. CTI in Seattle, WA Hauptsitz. Für weitere Informationen und zur Anmeldung für E-Mail-Benachrichtigungen und RSS-Feeds zu erhalten, besuchen Sie bitte die Website des Unternehmens auf www.CellTherapeutics.com .
Kontakte:
Monique Greer
+1 206-272-4343
mgreer@ctiseattle.com
Ed Bell-
+1 206.282.7100
ebell@ctiseattle.com
In Europa
CTI Life Sciences Limited, Niederlassung Mailand
Laura Villa
T: +39 02 89659706
E: lvilla @ CTI-lifesciences.com
CTI_EUInvestors@CTI-Lifesciences.com
SOURCE Cell Therapeutics, Inc.
Quelle: PR Newswire
13.01.14 12:55
#937
Rentnerzock
da kommt PLUS
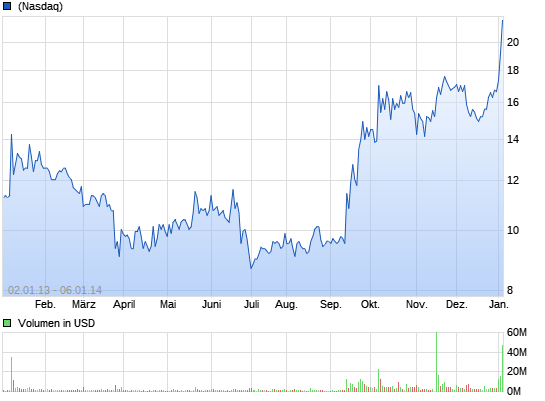
Heute legt die Aktie stark zu mit mehr als 14%. Stark.Kauf bei 0,99€ am 16.9.13 das sind 2,23€ mehr als 100%. Guter Kauf und Riecher. Gekauft habe ich die Aktie, weil ihr Kurs schon frühzeitig die 200TDL von unten nach oben durchschnitten hat. Es ist noch reichlich
Luft nach oben da.
Luft nach oben da.
13.01.14 22:21
#939
camerun
Es war wieder mal Nett.
In diesem Jahr mal knapp 1$ zugelegt.
Und das Jahr ist noch jung.
Und das Jahr ist noch jung.
15.01.14 17:59
#943
Balu4u
Gegen eine Erholungspause
gegen Überhitzung hab ich absolut nichts einzuwenden. Wenn man sich deren Portfolio so ansieht sehe ich noch genug Potential nach oben!
16.01.14 15:16
#944
camerun
Sieht wieder verdammt gut aus.
Die will doch wohl nicht weiterklettern?
17.01.14 12:55
#948
Balu4u
Ja, es läuft
denke es denken Einige ähnlich wie ich: Dass hier dank der Pipeline und guten Aufstellung noch Potential nach oben ist!? Wenn mich mir z.B. Ariad ansehe, bei der ich auch mal gezockt habe....die haben nur eine Medikament und eine MK von knapp 1 Mrd. Daher bin ich auch wegen des großen Risikos bei Ariad wieder raus und hab den Gewinn hier investiert. Denke, dass das ne gute Entscheidung war. Hier bin ich relaxter als bei Ariad.